Lösung zu Luftspeicher: Unterschied zwischen den Versionen
Erscheinungsbild
Inhalt gelöscht Inhalt hinzugefügt
Admin (Diskussion | Beiträge) Keine Bearbeitungszusammenfassung |
Admin (Diskussion | Beiträge) Keine Bearbeitungszusammenfassung |
||
| Zeile 1: | Zeile 1: | ||
<gallery> |
|||
Bild:Luftspeicher T-S-Diagramm.gif|''T-S-''Diagramm |
|||
Bild:Luftspeicher p-V-Diagramm.gif|''p-V-''Diagramm |
|||
</gallery> |
|||
#Im ''T-S-''Diagramm bilden die Isentropen vertikale Linien, die Isochoren verlaufen exponentiell in Funktion der Entropie oder logarithmisch mit der Temperatur. Im ''p-V-''Diagramm schneiden die Isentropen die Isothermen unter einem spitzen Winkel, die Isochoren verlaufen vertikal. |
#Im ''T-S-''Diagramm bilden die Isentropen vertikale Linien, die Isochoren verlaufen exponentiell in Funktion der Entropie oder logarithmisch mit der Temperatur. Im ''p-V-''Diagramm schneiden die Isentropen die Isothermen unter einem spitzen Winkel, die Isochoren verlaufen vertikal. |
||
#Am Ende des ersten Prozesses beträgt der Druck <math>p_2=p_1\left(\frac {V_1}{V_2}\right)^\kappa</math> = 6.96 bar und die Temperatur ist gleich <math>T_2=T_1\frac{p_2V_2}{p_1V_1}</math> = 522 K. Nach dem dritten Prozess beträgt der Druck nur noch 0.574 bar und die Temperatur misst 172 K. Für die Berechnung dieser Werte geht man am besten vom Anfangs- bzw. Endzustand aus und rechnet dann über die Isentrope rückwärts. |
#Am Ende des ersten Prozesses beträgt der Druck <math>p_2=p_1\left(\frac {V_1}{V_2}\right)^\kappa</math> = 6.96 bar und die Temperatur ist gleich <math>T_2=T_1\frac{p_2V_2}{p_1V_1}</math> = 522 K. Nach dem dritten Prozess beträgt der Druck nur noch 0.574 bar und die Temperatur misst 172 K. Für die Berechnung dieser Werte geht man am besten vom Anfangs- bzw. Endzustand aus und rechnet dann über die Isentrope rückwärts. |
||
Version vom 4. April 2008, 09:44 Uhr
-
T-S-Diagramm
-
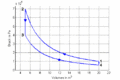
p-V-Diagramm
- Im T-S-Diagramm bilden die Isentropen vertikale Linien, die Isochoren verlaufen exponentiell in Funktion der Entropie oder logarithmisch mit der Temperatur. Im p-V-Diagramm schneiden die Isentropen die Isothermen unter einem spitzen Winkel, die Isochoren verlaufen vertikal.
- Am Ende des ersten Prozesses beträgt der Druck [math]\displaystyle{ p_2=p_1\left(\frac {V_1}{V_2}\right)^\kappa }[/math] = 6.96 bar und die Temperatur ist gleich [math]\displaystyle{ T_2=T_1\frac{p_2V_2}{p_1V_1} }[/math] = 522 K. Nach dem dritten Prozess beträgt der Druck nur noch 0.574 bar und die Temperatur misst 172 K. Für die Berechnung dieser Werte geht man am besten vom Anfangs- bzw. Endzustand aus und rechnet dann über die Isentrope rückwärts.
- Die Arbeit bei den isentropen Prozessen ist gleich der Änderung der inneren Energie. Diese hängt wiederum nur von der Temperatur ab [math]\displaystyle{ W_{tot}=W_{12}+W_{23}=n\hat c_V(T_2-T_1+T_4-T_3)=n\hat c_V(T_2+T_4-2T_1) }[/math] = 1.57 MJ.
- Im zweiten Teilprozess, der isochoren Auskühlung, beträgt die Änderung der inneren Energie [math]\displaystyle{ \Delta W=n\hat c_V(T_3-T_2) }[/math] = -3.7 MJ. Die zugehörige Entropieänderung ist gleich [math]\displaystyle{ \Delta S=n\hat c_V\ln\left(\frac{T_3}{T_2}\right) }[/math] = -9.2 kJ/K.