Lösung zu Kreisprozess mit Helium
Erscheinungsbild
-
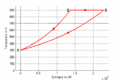
T-S-Diagramm
-
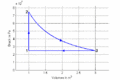
p-V-Diagramm
- Im T-S-Diagramme verläuft die isochore Zustandsänderung exponentiell nach oben, die isotherme horizontal und die isobare wiederum exponentiell und weniger steil zurück zum Ausgangspunkt. Im p-V-Diagramm steigt die Kurve zuerst vertikal nach oben, läuft dann auf einer Hyperbel ([math]\displaystyle{ pV=p_0V_0 }[/math]) nach rechts unten und zum Schluss auf einer Horizontalen nach links. Im T-S-Diagramm entspricht die Fläche unter der Kurve eines Teilprozesses der Wärme. Im p-V-Diagramm ergibt die entsprechende Fläche die (negativ genommene) Arbeit.
- Das universelle Gasgesetz liefert für den unteren Druck einen Wert von p1 = n * R * T1 / V1 = 10 kmol * 8.31 J/K/mol * 300 K / 1 m3 = 249 bar. Der Druck nach dem Aufheizen (1. Teilprozess) beträgt p2 = n * R * T2 / V2 = 10 kmol * 8.31 J/K/mol * 900 K / 1 m3 = 748 bar. Das Volumen beträgt nach dem zweiten, isothermen Teilprozess V3 = p2 / p3 * V2 = 748 bar / 249 bar * 1 m3 = 3 m3.
- Im ersten Teilprozess nimmt die Entropie um [math]\displaystyle{ \Delta S_{12}=n\hat c_V\ln{\frac{T_2}{T_1}}=\frac 3 2 nR\ln{\frac{T_2}{T_1}} }[/math] = 1.5 * 10 kmol * 8.31 J/K/mol * ln(900 K / 300 K) = 137 kJ/K zu. Im dritten, isobaren Teilprozess nimmt die Entropie um 5/3 dieses Wertes, also um 228 kJ/K ab, weil die Wärmekapazität bei konstantem Druck 5/3 der Wärmekapazität bei konstantem Volumen ist. Die Differenz von 91 kJ/K muss im zweiten, isothermen Teilprozess aus einem Wärmebad zugeführt werden.
- Im ersten, isochoren Teilprozess wird dem Helium die thermische Energie [math]\displaystyle{ W_{therm12} = n \hat c_V \Delta T }[/math] = 10 kmol * 1.5 * 8.31 J/K/mol * 600 K = 74.8 MJ zugeführt. Bei der nachfolgenden isothermen Zustandsänderung nimmt das Gas zusätzlich die thermische Energie [math]\displaystyle{ W_{therm23} = T_2 \Delta S_{23} = T_2 n R \ln{\frac{V_3}{V_2}} }[/math] = 900 K * 10 kmol * 8.31 J/K/mol * ln(3 m3 / 1 m3) = 82.2 MJ auf. Um die Energie für diese beiden Teilprozesse aus dem Ofen abzutransportieren, muss der Ofen die folgende Entropiemenge bei seiner konstanten Temperatur von 1000 K abgeben: [math]\displaystyle{ S_{Ofen}=\frac{W_{therm12} + W_{therm23}}{T_{Ofen}}=\frac{74.8 MJ + 82.2 MJ}{1000 K} }[/math] = 157 kJ/K. Im dritten, isobaren Teilprozess gibt das Helium die thermische Energie [math]\displaystyle{ W_{therm31} = n \hat c_p \Delta T = n \frac 5 2 R \Delta T }[/math] = 10 kmol * 2.5 * 8.31 J/K/mol * 600 K = 125 MJ ab. Diese Energie muss bei einer Temperatur von 280 K von der Entropie [math]\displaystyle{ S_{Um}=\frac{W_{therm31}}{T_{Um}} }[/math] = 125 MJ / 280 K = 446 kJ/K in die Umwelt hinein getragen werden. Erzeugt wird die Differenz zwischen der von Umwelt aufgenommenen und der vom Ofen abgegebenen Entropie. Diese Differenz beträgt 289 kJ/K.