Entropie und Enthalpie: Unterschied zwischen den Versionen
Admin (Diskussion | Beiträge) |
Admin (Diskussion | Beiträge) |
||
| Zeile 75: | Zeile 75: | ||
==Wärme, innere Energie und Enthalpie== |
==Wärme, innere Energie und Enthalpie== |
||
===Wärme=== |
|||
Die Energie, die thermisch, also zusammen mit der Entropie über die Systemgrenze transportiert wird, heisst Wärme. Die [[Wärme]] hängt wie die [[Kraft]] mit einem Transport über die Systemoberfläche zusammen. Folglich gibt es in der Physik weder einen Wärmeinhalt noch eine Umwandlung von nutzbarer Energie in Wärme. |
Die Energie, die thermisch, also zusammen mit der Entropie über die Systemgrenze transportiert wird, heisst Wärme. Die [[Wärme]] hängt wie die [[Kraft]] mit einem Transport über die Systemoberfläche zusammen. Folglich gibt es in der Physik weder einen Wärmeinhalt noch eine Umwandlung von nutzbarer Energie in Wärme. Als Formelzeichen wird für die Wärme oft ein ''Q'' geschrieben und für den Wärmestrom <math>\dot Q</math>. Weil wir in einer Bilanzgleichung den Punkt über einem Formelzeichen nur für die Änderungsrate verwenden und einer physikalischen Grösse möglichst immer mit das gleiche Formelzeichen zuweisen, schreiben wir für Wärme ''W<sub>therm</sub>'' und für die Stärke eines Wärmestromes bezüglich einer Referenzfläche ''I<sub>W_therm</sub>''. |
||
===innere Energie=== |
===innere Energie=== |
||
Die Energie, die in einem ruhenden System gespeichert ist, nennt man [[innere Energie]]. Das oft verwendete Formelzeichen für die innere Energie ist ''U''. Wir schreiben weiterhin ''W'' für die Energie. Gemäss ''Albert Einstein'' ist die innere Energie gleich Masse mal das Quadrat der Lichtgeschwindigkeit. Weil |
Die Energie, die in einem ruhenden System gespeichert ist, nennt man [[innere Energie]]. Das oft verwendete Formelzeichen für die innere Energie ist ''U''. Wir schreiben weiterhin ''W'' für die Energie. Gemäss ''Albert Einstein'' ist die innere Energie gleich Masse mal das Quadrat der Lichtgeschwindigkeit. Weil die Einsteinsche Gleichsetzung von Masse und Energie einen unbrauchbar grossen Wert liefert, setzt man die innere Energie bei einem ausgewählten Zustand (Druck, Temperatur, Aggregatszustand) gleich Null. Im Gegensatz zur inneren Energie sind die [[Bewegungsenergie]] ([[kinetische Energie]] und [[Rotationsenergie]]) und die potentielle Energie äussere Energieformen. So hängen die kinetische Energie (zusammen mit dem [[Impuls]] gespeichert) und die Rotationsenegie (zusammen mit dem [[Drehimpuls]] gespeichert) vom Bewegungszustand des Beobachters ([[Bezugssystem]]) ab. Die potentielle Energie steckt im [[Gravitationsfeld]] bzw. im [[elektromagnetisches Feld|elektromagnetischen Feld]] und wird nur formal dem Körper zugerechnet. |
||
===Enthalpie=== |
===Enthalpie=== |
||
| Zeile 97: | Zeile 98: | ||
:<math>W_{therm}=\Delta H</math> |
:<math>W_{therm}=\Delta H</math> |
||
Diese Gleichung erklärt auch das Wort Enthalpie (griech. ''en'' „darin, innerhalb” und ''thalpos'' „Wärme“). Das Wort Enthalpie ist ein schönes Beispiel akademischer Unaufrichtigkeit. Weil man '''Wärme als thermisch ausgetauschte Energie''' definiert hat, aber trotzdem den Begriff Wärmeinhalt beibehalten möchte, nimmt man einfach das griechische Wort. Der Buchstabe ''H'' kommt übrigens vom englischen Wort ''heat content''. |
Diese Gleichung erklärt auch das Wort Enthalpie (griech. ''en'' „darin, innerhalb” und ''thalpos'' „Wärme“): beim isobaren Heizen entspricht die Enthalpieänderung der zugeführten Wärme; kühlt man bei gleichem Druck um die gleiche Temperaturdifferenz ab, ändert das System seine Enthalpie wieder um den gleichen Betrag und gibt diese Energiemenge in Form von Wärme ab, . Das Wort Enthalpie ist ein schönes Beispiel akademischer Unaufrichtigkeit. Weil man '''Wärme als thermisch ausgetauschte Energie''' definiert hat, aber trotzdem den Begriff Wärmeinhalt beibehalten möchte, nimmt man einfach das griechische Wort. Der Buchstabe ''H'' kommt übrigens vom englischen Wort ''heat content''. |
||
Die Enthalpie ist ein reiner Hilfsbegriff mit der Einheit Joule. Beim isobaren Heizen oder Kühlen fasst die Änderung der Enthalpie die Änderung der inneren Energie und die Expansions- bzw. Kompressionsarbeit in einem Ausdruck zusammen. |
Die Enthalpie ist ein reiner Hilfsbegriff mit der Einheit Joule. Beim isobaren Heizen oder Kühlen fasst die Änderung der Enthalpie die Änderung der inneren Energie und die Expansions- bzw. Kompressionsarbeit in einem Ausdruck zusammen. |
||
Version vom 19. Januar 2008, 11:30 Uhr
Heizen heisst Entropie zuführen und zum Kühlen muss man Entropie abführen. Trotzdem hat man Mitte des neunzehnten Jahrhunderts die beim Heizen und Kühlen mit transportierte Energie als Wärme definiert. Der Grund für diese aus heutiger Sicht verfehlte Definition liegt bei der Entropie selber. Um dies zu verdeutlichen, vergleichen wir zwei analoge Prozesse
- Stossen zwei Autos frontal aufeinander, fliesst der Impuls von einem Auto ins andere, bis sich die Geschwindigkeiten angeglichen haben. In den Knautschzonen wird mit der vom Impuls freigesetzten Energie Entropie erzeugt.
- Giesst man kaltes und warmes Wasser in einem isolierten Mischgefäss (Kalorimeter) zusammen, überträgt das heisse Wasser einen Teil seiner Entropie ans kalte. In der Mischzone wird mit der von der Entropie freigesetzten Energie zusätzlich Entropie erzeugt.
Der Impuls bleibt erhalten und die mechanisch verfügbare Energie nimmt ab, derweil die Entropie zunimmt und die thermisch verfügbare Energie erhalten bleibt. Die Formel Wärme gleich Energie hat sich gegen die viel tiefgründigere Identifikation Wärme gleich Entropie durchgesetzt, weil man früher gemeint hat, eine bilanzierfähige (mengenartige) Grösse müsse auch erhalten sein.
In dieser Vorlesung wollen wir uns mit der Energie und der Entropie homogener Speicher beschäftigen.
Lernziele
Bilanzgleichungen
Führt man einem System Wärme zu oder ab, kann bezüglich des Systems eine Entropiebilanz aufgestellt werden
- [math]I_S=\dot S[/math]
Ist das System homogen, herrscht also an der Systemoberfläche die gleich Temperatur wie im Innern, darf die ganze Gleichung mit dieser (absoluten) Temperatur multipliziert werden. Links steht dann der zugeordnete Energiestrom, also nach offizieller Lesart der Wärmestrom, und rechts die Änderungsrate der inneren Energie
- [math]I_{W_{therm}}=\dot W[/math]
Diese Energiebilanz ist korrekt, falls das Volumen des Systems konstant bleibt. Man spricht dann vom isochoren Heizen (griech. choros für Tanzplatz). Heizt man dagegen bei konstantem Druck, nennt man den Vorgang isobar. In der Regel tauscht ein Stoff beim isobaren Heizen auch noch mechanische Energie mit der Umgebung aus. Die Energiebilanz umfasst dann mindestens drei Terme, einen thermischen und einen mechanischen Energiestrom sowie die Änderungsrate der inneren Energie. In dieser allgemeineren Form heisst die Energiebilanz auch erster Hauptsatz der Thermodynamik.
Carnotor
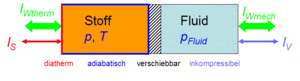
Wärmekraftmaschinen und Wärmepumpen arbeiten mit Stoffen die gasförmig oder zum Teil flüssig sind. Dabei spielen Expansion und Kompression sowie Heizen und Kühlen eine wesentliche Rolle. Um diese Prozesse kontrolliert ablaufen lassen, stellen wir uns ein Gerät, Carnotor genannt, vor. Dieses ideale Gerät besteht aus einem Doppelzylinder mit reibungsfrei verschiebbarem Kolben. Auf der einen Seite befindet sich der zu untersuchende, flüssige oder gasförmige Stoff. Die andere Seite ist mit einer inkompressiblen Hydraulikflüssigkeit gefüllt. Zylinderwand und Kolben sind adiabatisch (absolut wärmeundurchlässig), der Zylinderboden ist diatherm (ideal wärmedurchlässig). Nun kann man den Stoff heizen oder kühlen bzw. komprimieren oder dekomprimieren.
Vier Basisprozesse
Zum besseren Verständnis stellen wir uns vor, dass die Hydraulikflüssigkeit mit einer Pumpe und die Entropie mit einer Wärmepumpe hinein oder heraus gefördert wird. Vier Prozesse sind nun einfach zu realisieren
| Name | Wärmepumpe | Hydraulikpumpe | Vorgang |
|---|---|---|---|
| isochor | in Betrieb | blockiert | Heizen oder Kühlen |
| isobar | in Betrieb | Freilauf | Heizen oder Kühlen |
| isentrop | blockiert | in Betrieb | Komprimieren oder Expandieren |
| isotherm | Freilauf | in Betrieb | Komprimieren oder Expandieren |
Der Zustand "in Betrieb" bedeutet, dass die entsprechende Pumpe einen Strom erzeugt, also aktiv eine bestimmte Menge fördert. Im Zustand "blockiert" geht überhaupt kein Strom durch. Im "Freilauf" gleicht sich die Temperatur bzw. der Druck dem äusseren Potenzial an. In dieser Vorlesung beschäftigen wir uns nur mit dem isobaren Heizen bzw. Kühlen. Dabei wird Entropie zu- bzw. abgeführt und der Kolben hält einen bestimmten Druck aufrecht.
Änderungsraten
Bezüglich des (idealisierten Carnotors darf eine einfache Energiebilanz aufgestellt werden
- [math]I_{W_{therm}}+I_{W_{hyd}}=TI_S+pI_V=\dot W[/math]
Weil zwischen Zufuhr und Speicherung mangels Temperaturgefälle keine Entropie erzeugt, gilt eine einfache Entropiebilanz
- [math]I_S=\dot S[/math]
Die Volumenbilanz erstreckt sich auf zwei Kammern, wobei die Summe der beiden Änderungsrate immer gleich Null ist
- [math]I_V=\dot V_{hyd}=-\dot V[/math]
Der Freilauf der Hydraulikpumpe und der reibungsfrei verschiebbare Kolben sorgen für eine homogene Druckverteilung. Weil zudem die Temperatur im ganzen Bilanzgebiet gleich gross ist, dürfen die Volumen- und die Entropiebilanz in die Energiebilanz eingesetzt werden
- [math]T\dot S-p\dot V=\dot W[/math]
Diese Formel verknüpft die Änderung der inneren Energie mit den Änderungen der beiden mengenartigen Grössen Volumen und Entropie.
Wärme, innere Energie und Enthalpie
Wärme
Die Energie, die thermisch, also zusammen mit der Entropie über die Systemgrenze transportiert wird, heisst Wärme. Die Wärme hängt wie die Kraft mit einem Transport über die Systemoberfläche zusammen. Folglich gibt es in der Physik weder einen Wärmeinhalt noch eine Umwandlung von nutzbarer Energie in Wärme. Als Formelzeichen wird für die Wärme oft ein Q geschrieben und für den Wärmestrom [math]\dot Q[/math]. Weil wir in einer Bilanzgleichung den Punkt über einem Formelzeichen nur für die Änderungsrate verwenden und einer physikalischen Grösse möglichst immer mit das gleiche Formelzeichen zuweisen, schreiben wir für Wärme Wtherm und für die Stärke eines Wärmestromes bezüglich einer Referenzfläche IW_therm.
innere Energie
Die Energie, die in einem ruhenden System gespeichert ist, nennt man innere Energie. Das oft verwendete Formelzeichen für die innere Energie ist U. Wir schreiben weiterhin W für die Energie. Gemäss Albert Einstein ist die innere Energie gleich Masse mal das Quadrat der Lichtgeschwindigkeit. Weil die Einsteinsche Gleichsetzung von Masse und Energie einen unbrauchbar grossen Wert liefert, setzt man die innere Energie bei einem ausgewählten Zustand (Druck, Temperatur, Aggregatszustand) gleich Null. Im Gegensatz zur inneren Energie sind die Bewegungsenergie (kinetische Energie und Rotationsenergie) und die potentielle Energie äussere Energieformen. So hängen die kinetische Energie (zusammen mit dem Impuls gespeichert) und die Rotationsenegie (zusammen mit dem Drehimpuls gespeichert) vom Bewegungszustand des Beobachters (Bezugssystem) ab. Die potentielle Energie steckt im Gravitationsfeld bzw. im elektromagnetischen Feld und wird nur formal dem Körper zugerechnet.
Enthalpie
In unserer Umwelt hält die Luft den Druck konstant. Folglich laufen die meisten Heiz- oder Kühlvorgänge bei konstantem Druck, also isobar, ab. Untersucht man das isobare Heizen im Carnotor, stellt man fest, dass sich der Kolben durch die temperaturbedingte Ausdehnung bewegt und die Hydraulikflüssigkeit verdrängt. Die damit abgeführte Energie nennt man Expansionsarbeit. Weil man sich in diesem Fall nur für die Heizenergie interessiert, schreibt man die Energiebilanz um
- [math]I_{W_{therm}}=\dot W-I_{W_{hyd}}=\dot W+p\dot V[/math]
Um diese Bilanz zu vereinfachen, definieren wir eine neue Energiegrösse, die Enthalpie H
- [math]H=W+pV[/math]
Leitet man die Enthalpe bei konstantem Druck nach der Zeit ab, erhält man den rechten Term in der oben formulierten Energiebilanz
- [math]I_{W_{therm}}=\dot H[/math]
Heizt man ein System bei konstantem Druck auf, ist die zugeführte Energie gleich der Änderung der Enthalpie
- [math]W_{therm}=\Delta H[/math]
Diese Gleichung erklärt auch das Wort Enthalpie (griech. en „darin, innerhalb” und thalpos „Wärme“): beim isobaren Heizen entspricht die Enthalpieänderung der zugeführten Wärme; kühlt man bei gleichem Druck um die gleiche Temperaturdifferenz ab, ändert das System seine Enthalpie wieder um den gleichen Betrag und gibt diese Energiemenge in Form von Wärme ab, . Das Wort Enthalpie ist ein schönes Beispiel akademischer Unaufrichtigkeit. Weil man Wärme als thermisch ausgetauschte Energie definiert hat, aber trotzdem den Begriff Wärmeinhalt beibehalten möchte, nimmt man einfach das griechische Wort. Der Buchstabe H kommt übrigens vom englischen Wort heat content.
Die Enthalpie ist ein reiner Hilfsbegriff mit der Einheit Joule. Beim isobaren Heizen oder Kühlen fasst die Änderung der Enthalpie die Änderung der inneren Energie und die Expansions- bzw. Kompressionsarbeit in einem Ausdruck zusammen.